Pfizer-ի mRNA պատվաստանյութը COVID-ի դեմ կրկին բորբոքել է կիրքը ռիբոնուկլեինաթթու (ՌՆԹ) որպես բուժական թիրախ օգտագործելու համար:Այնուամենայնիվ, փոքր մոլեկուլներով ՌՆԹ-ի թիրախավորումը չափազանց դժվար է:
ՌՆԹ-ն ունի միայն չորս շինանյութ՝ ադենին (A), ցիտոզին (C), գուանին (G) և ուրացիլ (U), որը փոխարինում է ԴՆԹ-ում հայտնաբերված թիմինին (T):Սա դեղերի ընտրողականությունը դարձնում է գրեթե անհաղթահարելի խոչընդոտ:Ի հակադրություն, կան 22 բնական ամինաթթուներ, որոնք կազմում են սպիտակուցները, ինչը բացատրում է, թե ինչու են սպիտակուցներին ուղղված դեղամիջոցների մեծ մասը համեմատաբար լավ ընտրողականություն:
ՌՆԹ-ի կառուցվածքը և գործառույթը
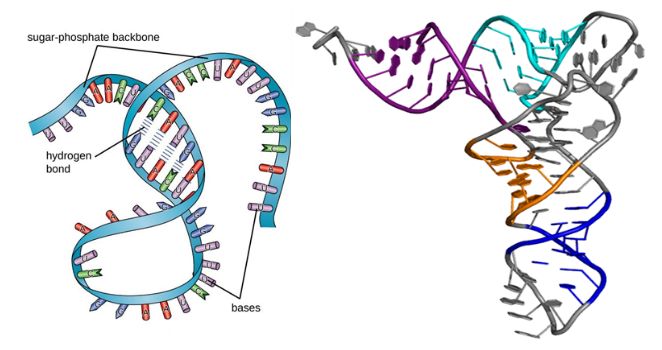
Ինչպես սպիտակուցները, ՌՆԹ-ի մոլեկուլներն ունեն երկրորդական և երրորդական կառուցվածքներ, ինչպես ցույց է տրված ստորև նկարում:Թեև դրանք միաշղթայով մակրոմոլեկուլներ են, նրանց երկրորդական կառուցվածքը ձևավորվում է, երբ հիմքերի զուգավորումն առաջացնում է ուռուցիկություն, օղակ և պարույր:Այնուհետև եռաչափ ծալումը հանգեցնում է ՌՆԹ-ի երրորդական կառուցվածքին, որն էական նշանակություն ունի նրա կայունության և գործունեության համար:
Նկար 1. ՌՆԹ-ի կառուցվածքը
ՌՆԹ-ի երեք տեսակ կա.
- Մեսսենջեր ՌՆԹ (mRNA)արտագրում է գենետիկական տեղեկատվությունը ԴՆԹ-ից և որպես բազային հաջորդականություն փոխանցվում է ռիբոսոմի վրա.լ
- Ռիբոսոմային ՌՆԹ (rRNA)սպիտակուցներ սինթեզող օրգանելների մի մասն է, որը կոչվում է ռիբոսոմներ, որոնք արտահանվում են ցիտոպլազմա և օգնում են թարգմանել տեղեկատվությունը mRNA-ում սպիտակուցների;
- Տրանսֆերային ՌՆԹ (tRNA)կապն է mRNA-ի և ամինաթթուների շղթայի միջև, որը կազմում է սպիտակուցը:
ՌՆԹ-ի թիրախավորումը որպես թերապևտիկ թիրախ շատ գրավիչ է:Պարզվել է, որ մեր գենոմի միայն 1,5%-ն է ի վերջո վերածվում սպիտակուցի, մինչդեռ 70%-90%-ը տառադարձվում է ՌՆԹ-ի:ՌՆԹ-ի մոլեկուլները ամենակարևորն են բոլոր կենդանի օրգանիզմների համար:Ըստ Ֆրենսիս Քրիքի «կենտրոնական դոգմայի»՝ ՌՆԹ-ի ամենակարևոր դերը ԴՆԹ-ից գենետիկ տեղեկատվությունը սպիտակուցների վերածելն է:Բացի այդ, ՌՆԹ-ի մոլեկուլներն ունեն նաև այլ գործառույթներ, այդ թվում՝
- Գործելով որպես ադապտերային մոլեկուլներ սպիտակուցի սինթեզում;լ
- Ծառայելով որպես սուրհանդակ ԴՆԹ-ի և ռիբոսոմի միջև;լ
- Նրանք գենետիկ տեղեկատվության կրողներ են բոլոր կենդանի բջիջներում.լ
- Նպաստել ճիշտ ամինաթթուների ռիբոսոմային ընտրությանը, որն անհրաժեշտ է նոր սպիտակուցներ սինթեզելու համարin vivo.
Հակաբիոտիկներ
Չնայած հայտնաբերմանը դեռևս 1940-ականներին, շատ հակաբիոտիկների գործողության մեխանիզմը պարզաբանված չէր մինչև 1980-ականների վերջը:Պարզվել է, որ հակաբիոտիկների մեծ մասը գործում է բակտերիալ ռիբոսոմների հետ կապվելու միջոցով՝ կանխելով նրանց համապատասխան սպիտակուցներ արտադրելը, դրանով իսկ սպանելով բակտերիաները:
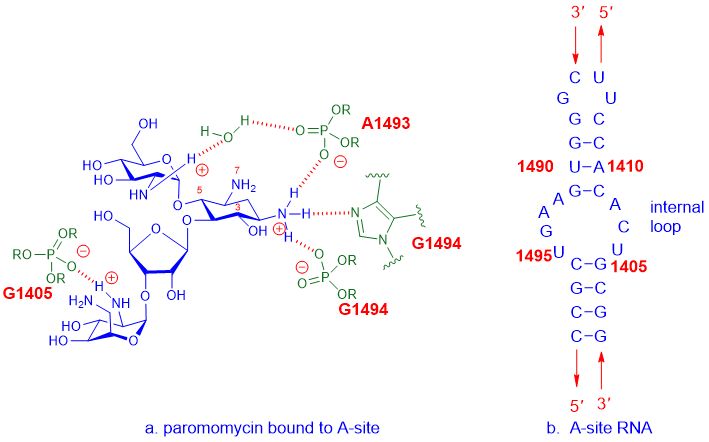
Օրինակ, ամինոգլիկոզիդային հակաբիոտիկները կապվում են 16S rRNA-ի A-կայքին, որը 30S ռիբոսոմի ենթամիավորի մի մասն է, այնուհետև խանգարում է սպիտակուցի սինթեզին՝ խանգարելով բակտերիաների աճին, ինչը, ի վերջո, հանգեցնում է բջիջների մահվան:A-կայքը վերաբերում է aminoacyl կայքին, որը նաև հայտնի է որպես tRNA ընդունող տեղ:Մանրամասն փոխազդեցությունը ամինոգլիկոզիդային դեղամիջոցների միջև, ինչպիսիք ենպարոմոմիցին, իսկ Ա-կայքըE. coliՌՆԹ-ն ներկայացված է ստորև:
Նկար 2. Փարոմոմիցինի և A-կայքի փոխազդեցությունըE. coliՌՆԹ
Ցավոք, A-site-ի շատ ինհիբիտորներ, ներառյալ ամինոգլիկոզիդային դեղամիջոցները, ունեն անվտանգության խնդիրներ, ինչպիսիք են նեֆրոտոքսիկությունը, դոզայից կախված և հատուկ անդառնալի օտոտոքսիկությունը:Այս թունավորությունը ՌՆԹ-ի փոքր մոլեկուլները ճանաչելու համար ամինոգլիկոզիդային դեղամիջոցների ընտրողականության պակասի արդյունք է:
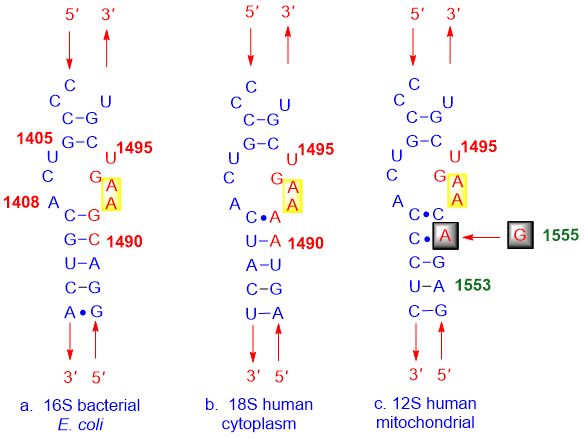
Ինչպես ցույց է տրված ստորև բերված նկարում.
Նկար 3. A-site inhibitor-ի ոչ ընտրովի կապը
Tetracycline հակաբիոտիկները նույնպես արգելակում են rRNA-ի A-կայքը:Նրանք ընտրողաբար արգելակում են բակտերիալ սպիտակուցի սինթեզը՝ շրջելիորեն կապվելով 30S ենթամիավորի պտուտակավոր շրջանին (H34)՝ կոմպլեքսավորված Mg-ով:2+.
Մյուս կողմից, մակրոլիդային հակաբիոտիկները կապվում են նորածին պեպտիդների (NPET) բակտերիալ ռիբոսոմային թունելի ելքի վայրի մոտ (E-site) և մասամբ արգելափակում այն՝ դրանով իսկ արգելելով բակտերիալ սպիտակուցի սինթեզը:Վերջապես, oxazolidinone հակաբիոտիկները, ինչպիսիք ենլինեզոլիդ(Zyvox) կապվում է բակտերիալ 50S ռիբոսոմային ենթամիավորի խորը ճեղքին, որը շրջապատված է 23S rRNA նուկլեոտիդներով։
Հակազգայուն օլիգոնուկլեոտիդներ (ASO)
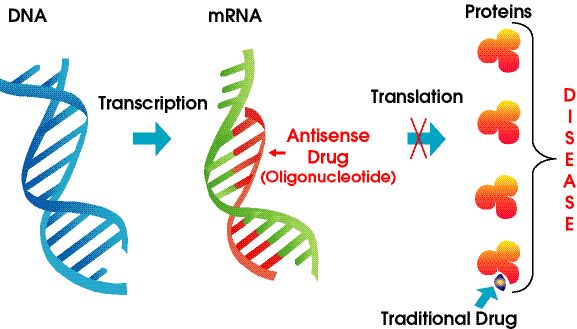
Հակասենսային դեղամիջոցները քիմիական ձևափոխված նուկլեինաթթուների պոլիմերներ են, որոնք թիրախավորում են ՌՆԹ-ն:Նրանք հիմնվում են Watson-Crick բազայի զուգակցման վրա՝ միանալու թիրախային mRNA-ին, ինչը հանգեցնում է գեների խլացման, ստերիկ շրջափակման կամ միացման փոփոխության:ASO-ները կարող են փոխազդել բջջի միջուկում գտնվող նախաՌՆԹ-ների հետ, իսկ ցիտոպլազմայում` հասուն մՌՆԹ-ների հետ:Նրանք կարող են թիրախավորել էկզոնները, ինտրոնները և չթարգմանված շրջանները (UTRs):Մինչ օրս մեկ տասնյակից ավելի ASO դեղամիջոցներ հաստատվել են FDA-ի կողմից:
Նկար 4. Antisense Technology
Փոքր մոլեկուլային դեղամիջոցներ, որոնք ուղղված են ՌՆԹ-ին
2015-ին Novartis-ը հայտնեց, որ իրենք հայտնաբերել են SMN2 միացման կարգավորիչ, որը կոչվում է Branaplam, որն ուժեղացնում է U1-pre-mRNA-ի կապը և փրկում SMA մկներին:
Մյուս կողմից, PTC/Roche-ի Risdiplam-ը (Evrysdi) հաստատվել է FDA-ի կողմից 2020 թվականին՝ SMA-ի բուժման համար:Ինչպես Branaplam-ը, Risdiplam-ը նույնպես աշխատում է՝ կարգավորելով համապատասխան SMN2 գեների միացումը՝ ֆունկցիոնալ SMN սպիտակուցներ արտադրելու համար:
ՌՆԹ դեգրադատորներ
RBM նշանակում է ՌՆԹ կապող մոտիվ սպիտակուց:Ըստ էության, ինդոլ սուլֆոնամիդը մոլեկուլային սոսինձ է:Այն ընտրողաբար ներգրավում է RBM39-ը CRL4-DCAF15 E3 ուբիկվիտին լիգազի մեջ՝ նպաստելով RBM39 պոլիուբիկվիտինացմանը և սպիտակուցի քայքայմանը:RBM39-ի գենետիկ սպառումը կամ սուլֆոնամիդով միջնորդավորված դեգրադացիան առաջացնում է գենոմի լայնածավալ զուգավորման զգալի շեղումներ, որոնք ի վերջո հանգեցնում են բջիջների մահվան:
ՌՆԹ-ՊՐՈՏԱԿ-ները մշակվում են ՌՆԹ կապող սպիտակուցները (RBP) քայքայելու համար:PROTAC-ն օգտագործում է կապակցիչ՝ E3 լիգազի լիգանդը ՌՆԹ-ի հետ կապելու համար, որը կապում է ՌՆԹ-ին և RBP-ներին:Քանի որ RBP-ն պարունակում է կառուցվածքային տիրույթներ, որոնք կարող են կապվել հատուկ օլիգոնուկլեոտիդային հաջորդականությունների հետ, ՌՆԹ-ՊՐՈՏԱԿ-ն օգտագործում է օլիգոնուկլեոտիդային հաջորդականությունը՝ որպես հետաքրքրող սպիտակուցի (POI) լիգանդ:Վերջնական արդյունքը ՌԲՊ-ների դեգրադացումն է:
Վերջերս Սկրիպսի օվկիանոսագիտության ինստիտուտի պրոֆեսոր Մեթյու Դիսնեյը հայտնագործեց ՌՆԹ-ն.ռիբոնուկլեազին ուղղված քիմերաներ (RiboTACs).RiboTAC-ը հետերոֆունկցիոնալ մոլեկուլ է, որը կապում է RNase L լիգանդը և ՌՆԹ-ի լիգանդը կապակցիչով:Այն կարող է հատուկ հավաքագրել էնդոգեն RNase L-ն հատուկ ՌՆԹ թիրախների, այնուհետև հաջողությամբ վերացնել ՌՆԹ-ն՝ օգտագործելով բջջային նուկլեինաթթվի քայքայման մեխանիզմը (RNase L):
Քանի որ հետազոտողները ավելի շատ են իմանում փոքր մոլեկուլների և ՌՆԹ թիրախների փոխազդեցության մասին, ապագայում այս մեթոդով ավելի շատ դեղամիջոցներ կհայտնվեն:
Հրապարակման ժամանակը՝ օգ-02-2023