Մոլեկուլային կենսաբանության տեխնոլոգիայի շարունակական զարգացման հետ մեկտեղ գենային մուտացիաների և արատների ու հիվանդությունների միջև կապը ավելի ու ավելի խորը պատկերացում է ստացել:Նուկլեինաթթուները մեծ ուշադրություն են գրավել հիվանդությունների ախտորոշման և բուժման մեջ կիրառման մեծ ներուժի պատճառով:Նուկլեինաթթվային դեղամիջոցները վերաբերում են արհեստականորեն սինթեզված ԴՆԹ-ի կամ ՌՆԹ-ի բեկորներին՝ հիվանդության բուժման գործառույթներով:Նման դեղամիջոցները կարող են ուղղակիորեն գործել հիվանդություն առաջացնող թիրախ գեների կամ հիվանդություն առաջացնող թիրախային mRNA-ների վրա և դեր խաղալ գեների մակարդակով հիվանդությունների բուժման գործում:Համեմատած ավանդական փոքր մոլեկուլային դեղամիջոցների և հակամարմինների դեղերի հետ՝ նուկլեինաթթվային դեղամիջոցները կարող են կարգավորել հիվանդություն առաջացնող գեների արտահայտումը արմատից և ունենալ «ախտանիշները բուժելու և արմատական պատճառը բուժելու» բնութագրերը:Նուկլեինաթթվային դեղամիջոցներն ունեն նաև ակնհայտ առավելություններ, ինչպիսիք են բարձր արդյունավետությունը, ցածր թունավորությունը և բարձր սպեցիֆիկությունը:Քանի որ առաջին նուկլեինաթթվային դեղամիջոցը fomivirsen sodium-ը գործարկվել է 1998 թվականին, նուկլեինաթթվային շատ դեղամիջոցներ հաստատվել են կլինիկական բուժման համար:
Ներկայումս համաշխարհային շուկայում նուկլեինաթթվային դեղամիջոցները հիմնականում ներառում են հակազգայուն նուկլեինաթթու (ASO), փոքր միջամտող ՌՆԹ (siRNA) և նուկլեինաթթու ապտամերներ:Բացառությամբ նուկլեինաթթուների ապտամերների (որոնք կարող են գերազանցել 30 նուկլեոտիդները), նուկլեինաթթվային դեղամիջոցները սովորաբար օլիգոնուկլեոտիդներ են՝ կազմված 12-ից 30 նուկլեոտիդներից, որոնք նաև հայտնի են որպես օլիգոնուկլեոտիդային դեղամիջոցներ:Բացի այդ, միՌՆԹ-ները, ռիբոզիմները և դեզօքսիռիբոզիմները նույնպես զարգացման մեծ արժեք են ցուցաբերել տարբեր հիվանդությունների բուժման գործում:Նուկլեինաթթվային դեղամիջոցներն այսօր դարձել են կենսաբժշկության հետազոտության և զարգացման ամենահեռանկարային ոլորտներից մեկը:
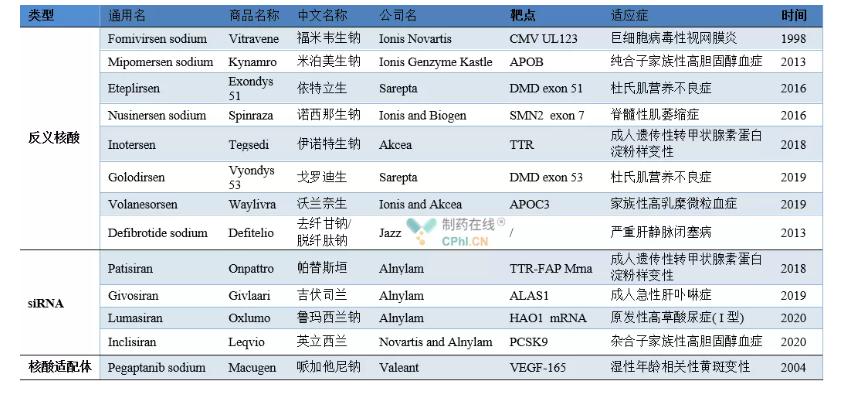
Հաստատված նուկլեինաթթվային դեղամիջոցների օրինակներ
Antisense նուկլեինաթթու
Antisense տեխնոլոգիան դեղամիջոցի մշակման նոր տեխնոլոգիա է, որը հիմնված է Watson-Crick բազայի լրացման սկզբունքի վրա՝ օգտագործելով օրգանիզմի կողմից արհեստականորեն սինթեզված կամ սինթեզված հատուկ կոմպլեմենտար ԴՆԹ կամ ՌՆԹ բեկորներ՝ նպատակային գեների էքսպրեսիան հատուկ կարգավորելու համար:Հակասենս նուկլեինաթթուն ունի թիրախային ՌՆԹ-ին լրացնող բազային հաջորդականություն և կարող է հատուկ կապվել դրան:Հակասենս նուկլեինաթթուները հիմնականում ներառում են հակասիտ ԴՆԹ, հակազգայական ՌՆԹ և ռիբոզիմներ:Դրանց թվում, հակազգայական ԴՆԹ-ի բարձր կայունության և ցածր գնի բնութագրերի շնորհիվ, հակազգայուն ԴՆԹ-ն գերիշխող դիրք է գրավում հակասիտային նուկլեինաթթուների ներկայիս հետազոտության և կիրառման մեջ:
Fomivirsen sodium (առևտրային անվանումը Vitravene) մշակվել է Ionis Novartis-ի կողմից:1998 թվականի օգոստոսին FDA-ն հաստատեց այն ցիտոմեգալովիրուսային ռետինիտի բուժման համար իմունային անբավարարված հիվանդների (հիմնականում ՁԻԱՀ-ով հիվանդների) համար՝ դառնալով առաջին նուկլեինաթթվային դեղամիջոցը, որը շուկա է հանվել:Fomivirsen-ն արգելակում է CMV-ի մասնակի սպիտակուցային արտահայտումը` կապվելով հատուկ mRNA-ին (IE2)՝ դրանով իսկ կարգավորելով վիրուսային գեների արտահայտումը բուժական ազդեցության հասնելու համար:Այնուամենայնիվ, բարձր արդյունավետ հակառետրովիրուսային թերապիայի առաջացման պատճառով, որը զգալիորեն նվազեցրեց հիվանդների թիվը, 2002 և 2006 թվականներին Novartis-ը չեղյալ հայտարարեց Fomivirsen դեղամիջոցների շուկայական թույլտվությունը համապատասխանաբար Եվրոպայում և Միացյալ Նահանգներում, և արտադրանքը կասեցվեց շուկայից:
Mipomersen sodium (առևտրային անվանումը Kynamro) ASO դեղամիջոց է, որը մշակվել է ֆրանսիական Genzyme ընկերության կողմից:2013 թվականի հունվարին FDA-ն այն հաստատեց հոմոզիգոտ ընտանեկան հիպերխոլեստերինեմիայի բուժման համար:Միպոմերսենը արգելակում է ApoB-100 սպիտակուցի (ապոլիպոպրոտեինի) արտահայտումը՝ կապվելով ApoB-100mRNA-ի հետ՝ դրանով իսկ զգալիորեն նվազեցնելով մարդու ցածր խտության լիպոպրոտեինի խոլեստերինը, ցածր խտության լիպոպրոտեինը և այլ ցուցիչներ, սակայն կողմնակի ազդեցությունների պատճառով, ինչպիսիք են լյարդի թունավորությունը, Դեկտեմբերի 12-ին, դեղի կրկնակի կիրառման լիցենզիա: .
2016 թվականի սեպտեմբերին Eteplirsen-ը (առևտրային անվանումը՝ Exon 51), որը մշակվել է Sarepta-ի կողմից Դյուշենի մկանային դիստրոֆիայի (DMD) բուժման համար, հաստատվել է FDA-ի կողմից:DMD հիվանդները սովորաբար չեն կարող արտահայտել ֆունկցիոնալ հակաատրոֆիկ սպիտակուցը մարմնում DMD գենի մուտացիաների պատճառով:Էտեպլիրսենը հատուկ կապվում է սպիտակուցի նախասեսսենջեր ՌՆԹ-ի (Pre-mRNA) էկզոն 51-ին, հեռացնում է էկզոն 51-ը և վերականգնում է ներքևում գտնվող որոշ գեներ:
Nusinersen-ը ASO դեղամիջոց է, որը մշակվել է Spinraza-ի կողմից՝ ողնաշարի մկանային ատրոֆիայի բուժման համար և հաստատվել է FDA-ի կողմից 2016 թվականի դեկտեմբերի 23-ին: 2018 թվականին Inotesen-ը, որը մշակվել է Tegsedi-ի կողմից՝ մեծահասակների ժառանգական տրանսթիրետինային ամիլոիդոզի բուժման համար, հաստատվել է FDA-ի կողմից:2019 թվականին Դյուշենի մկանային դիստրոֆիայի բուժման համար Sarepta-ի կողմից մշակված Golodirsen-ը հաստատվել է FDA-ի կողմից:Այն ունի գործողության նույն մեխանիզմը, ինչ Eteplirsen-ը, և դրա գործողության վայրը դառնում է էկզոն 53: Նույն թվականին Volanesorsen-ը, որը համատեղ մշակվել է Ionisand Akcea-ի կողմից ընտանեկան հիպերխիլոմիկրոնեմիայի բուժման համար, հաստատվել է Եվրոպական դեղամիջոցների գործակալության (EMA) կողմից:Volanesorsen-ը կարգավորում է տրիգլիցերիդների նյութափոխանակությունը՝ արգելակելով ապոլիպոպրոտեին C-Ⅲ արտադրությունը, սակայն այն նաև ունի թրոմբոցիտների մակարդակի իջեցման կողմնակի ազդեցություն:
Դեֆիբրոտիդը օլիգոնուկլեոտիդային խառնուրդ է՝ պլազմինային հատկություններով, որը մշակվել է Jazz-ի կողմից։Այն պարունակում է 90% ԴՆԹ միաշղթա ԴՆԹ և 10% ԴՆԹ երկշղթա:Այն հաստատվել է EMA-ի կողմից 2013 թվականին և այնուհետև հաստատվել է FDA-ի կողմից՝ լյարդի ծանր երակների բուժման համար:Օկլյուզիվ հիվանդություն.Դեֆիբրոտիդը կարող է մեծացնել պլազմինի ակտիվությունը, մեծացնել պլազմինոգենի ակտիվացնողը, խթանել թրոմբոմոդուլինի բարձրակարգ կարգավորումը և նվազեցնել ֆոն Վիլլեբրանդի գործոնի և պլազմինոգենի ակտիվացնողի ինհիբիտորների արտահայտվածությունը՝ հասնելու թերապևտիկ էֆեկտների։
siRNA
siRNA-ն որոշակի երկարությամբ և հաջորդականությամբ ՌՆԹ-ի փոքր բեկոր է, որն արտադրվում է թիրախ ՌՆԹ-ի կտրման միջոցով:Այս siRNA-ները կարող են հատուկ դրդել թիրախային mRNA-ի քայքայմանը և հասնել գենի խլացման էֆեկտների:Քիմիական փոքր մոլեկուլային դեղամիջոցների համեմատ, siRNA դեղամիջոցների գենը խլացնող ազդեցությունն ունի բարձր առանձնահատկություն և արդյունավետություն:
2018 թվականի օգոստոսի 11-ին առաջին siRNA դեղամիջոցը patisiran (առևտրային անվանումը՝ Onpattro) հաստատվեց FDA-ի կողմից և պաշտոնապես գործարկվեց:Սա ՌՆԹ-ի միջամտության տեխնոլոգիայի զարգացման պատմության կարևորագույն իրադարձություններից մեկն է:Patisiran-ը համատեղ մշակվել է Alnylam-ի և Genzyme-ի՝ Sanofi-ի դուստր ձեռնարկությունների կողմից:Դա siRNA դեղամիջոց է ժառանգական թիրոքսինով պայմանավորված ամիլոիդոզի բուժման համար:2019 թվականին givosiran-ը (ապրանքային անվանումը՝ Givlaari) FDA-ի կողմից հաստատվել է որպես մեծահասակների մոտ լյարդի սուր պորֆիրիայի բուժման երկրորդ siRNA դեղամիջոց:2020 թվականին Alnylam-ը մշակեց առաջնային տիպի I դեղամիջոց երեխաների և մեծահասակների բուժման համար:Բարձր օքսալուրիա ունեցող Lumasiran-ը հաստատվել է FDA-ի կողմից:2020 թվականի դեկտեմբերին Inclisiran-ը, որը համատեղ մշակվել է Novartis-ի և Alnylam-ի կողմից՝ մեծահասակների հիպերխոլեստերինեմիայի կամ խառը դիսլիպիդեմիայի բուժման համար, հաստատվել է EMA-ի կողմից:
Ապտամեր
Նուկլեինաթթուների ապտամերները օլիգոնուկլեոտիդներ են, որոնք կարող են կապվել տարբեր թիրախային մոլեկուլների հետ, ինչպիսիք են փոքր օրգանական մոլեկուլները, ԴՆԹ-ն, ՌՆԹ-ն, պոլիպեպտիդները կամ սպիտակուցները՝ բարձր կապակցությամբ և յուրահատկությամբ:Համեմատած հակամարմինների հետ՝ նուկլեինաթթուների ապտամերներն ունեն պարզ սինթեզի բնութագրեր, ավելի ցածր գնով և թիրախների լայն շրջանակով և ունեն ավելի լայն ներուժ դեղամիջոցների կիրառման համար հիվանդությունների ախտորոշման, բուժման և կանխարգելման մեջ:
Պեգապտանիբը նուկլեինաթթվի ապտամերային առաջին դեղամիջոցն է, որը մշակվել է Valeant-ի կողմից թաց տարիքային մակուլյար դեգեներացիայի բուժման համար և հաստատվել է FDA-ի կողմից 2004թ.-ին: Այնուհետև այն հաստատվել է EMA-ի և PMDA-ի կողմից 2006թ. հունվարին և 2008թ. հուլիսին և հայտնվել շուկայում:Պեգապտանիբը արգելակում է անգիոգենեզը տարածական կառուցվածքի և անոթային էնդոթելիային աճի գործոնի համակցման միջոցով՝ հասնելու թերապևտիկ ազդեցության:Այդ ժամանակից ի վեր, այն բախվել է նմանատիպ Lucentis դեղամիջոցների մրցակցությանը, և նրա մասնաբաժինը շուկայում զգալիորեն նվազել է:
Նուկլեինաթթվային դեղամիջոցները դարձել են թեժ կետ կլինիկական դեղերի և նոր դեղամիջոցների շուկայում՝ շնորհիվ իրենց ուշագրավ բուժիչ ազդեցության և զարգացման կարճ ցիկլի:Որպես զարգացող դեղամիջոց՝ այն բախվում է մարտահրավերների՝ հանդիպելով հնարավորություններին:Իր էկզոգեն բնութագրերի շնորհիվ նուկլեինաթթուների յուրահատկությունը, կայունությունը և արդյունավետ առաքումը դարձել են հիմնական չափանիշները դատելու համար, թե արդյոք օլիգոնուկլեոտիդները կարող են դառնալ բարձր արդյունավետ նուկլեինաթթու դեղամիջոցներ:Թիրախային ազդեցությունները միշտ եղել են նուկլեինաթթվային դեղամիջոցների հիմնական կետը, որը չի կարելի անտեսել:Այնուամենայնիվ, նուկլեինաթթվային դեղամիջոցները կարող են ազդել արմատից հիվանդություն առաջացնող գեների արտահայտման վրա և կարող են հասնել հաջորդականության յուրահատկության մեկ բազային մակարդակում, որն ունի «հիմնական պատճառի բուժման և ախտանիշների բուժման» առանձնահատկությունները:Հաշվի առնելով ավելի ու ավելի շատ հիվանդությունների փոփոխականությունը, միայն գենետիկական բուժումը կարող է հասնել մշտական արդյունքների:Հարակից տեխնոլոգիաների շարունակական բարելավմամբ, կատարելագործմամբ և առաջընթացով, նուկլեինաթթվային դեղամիջոցները, որոնք ներկայացված են հակասիտային նուկլեինաթթուներով, siRNA-ով և նուկլեինաթթու ապտամերներով, անկասկած, նոր ալիք կառաջացնեն հիվանդությունների բուժման և դեղագործական արդյունաբերության մեջ:
Rակնարկներ:
[1] Լյու Շաոջին, Ֆեն Սյուեջյաո, Վան Ջունշու, Սյաո Չժենգցյան, Չենգ Պինգշեն։Նուկլեինաթթվային դեղերի շուկայի վերլուծություն իմ երկրում և հակաքայլեր[J]:Կենսաբանական ճարտարագիտության չինական ամսագիր, 2021, 41 (07): 99-109:
[2] Չեն Վենֆեյ, Ու Ֆուհուա, Չժան Ժիրոնգ, Սուն Սյուն։Հետազոտության առաջընթացը շուկայահանվող նուկլեինաթթվային դեղերի դեղագիտության մեջ [J]:Չինական դեղագործական հանդես, 2020, 51 (12): 1487-1496:
[3] Վան Ջուն, Վան Լան, Լու Ցզյաժեն, Հուանգ Չժեն։Նուկլեինաթթուների շուկայահանվող դեղերի արդյունավետության և հետազոտության առաջընթացի վերլուծություն [J]:Նոր դեղերի չինական ամսագիր, 2019, 28 (18): 2217-2224:
Հեղինակի մասին Շա Լուոն, չինական բժշկության հետազոտման և մշակման աշխատող, ներկայումս աշխատում է դեղերի հետազոտման և մշակման խոշոր տեղական ընկերությունում և հավատարիմ է նոր չինական դեղամիջոցների հետազոտմանը և զարգացմանը:
Առնչվող ապրանքներ.
Հրապարակման ժամանակը՝ նոյ-19-2021